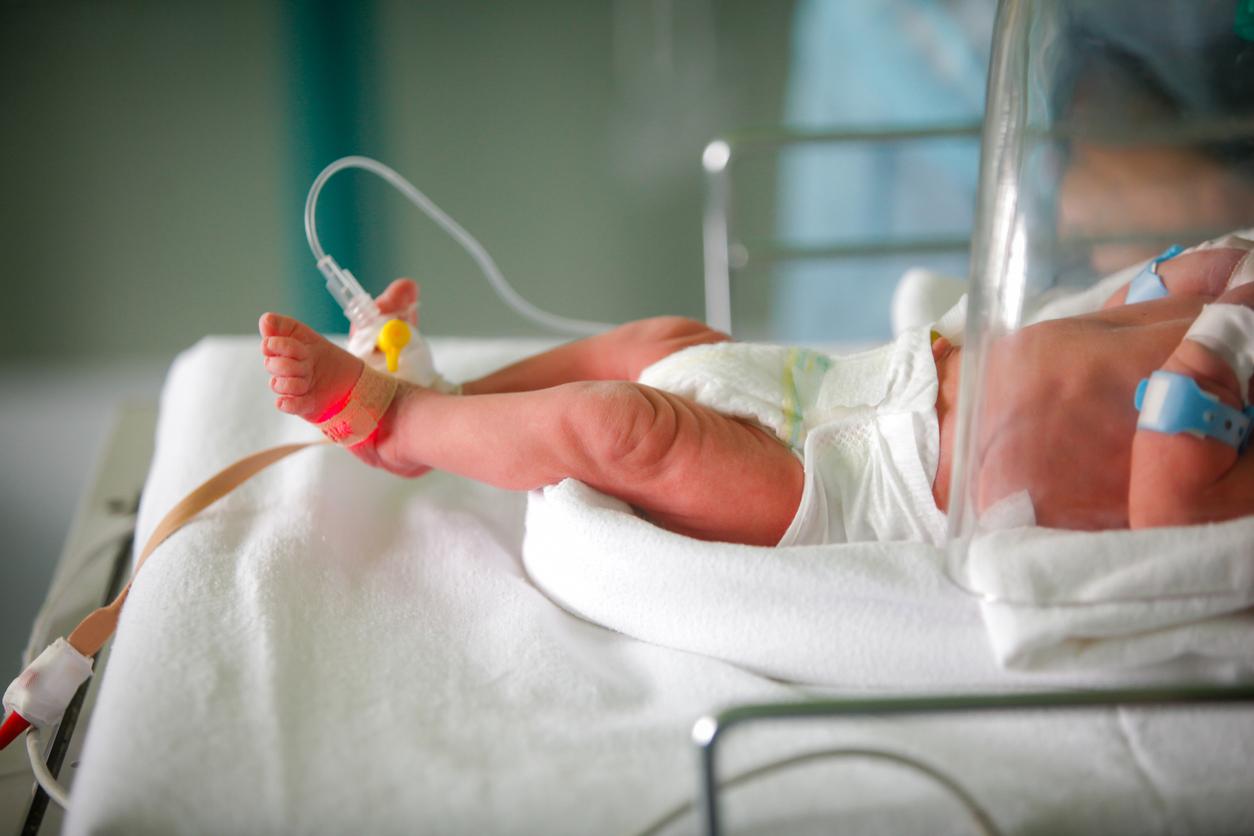
- Pfizer a mis au point un nouveau vaccin contre la bronchiolite pour les nourrissons et les personnes âgées.
- L’Agence européenne des médicaments vient de l'approuver.
- Le laboratoire va pouvoir faire une demande d’autorisation de mise sur le marché auprès de la Commission européenne.
Abrysvo, c’est le nom du premier vaccin contre le virus respiratoire syncytial (VRS), à l’origine de la bronchiolite, approuvé par l’Agence européenne des médicaments (EMA) pour les nourrissons. Plus précisément, celui-ci est indiqué pour l’immunisation passive de la naissance à six mois après l’administration du vaccin à la mère pendant la grossesse.
Un vaccin pour protéger les nourrissons et les personnes âgées
Ce vaccin, mis au point par le laboratoire Pfizer, est aussi “indiqué pour l’immunisation active des adultes âgés de 60 ans et plus”, explique l’EMA. L’Agence américaine des médicaments (La Food and Drug Administration - FDA) l’a d’ailleurs déjà approuvé pour les personnes âgées.
Mais, pour cette tranche d’âge, Abrysvo n’est pas le seul disponible. En effet, en juin dernier, le vaccin Arexvy, du laboratoire britannique GSK, a obtenu de la Commission européenne une autorisation de mise sur le marché dans l’Union européenne.
L’urgence était donc de mettre au point un vaccin capable de protéger les plus jeunes car, chaque hiver, 30% des nourrissons de moins de deux ans sont touchés par la bronchiolite selon Santé Publique France.
Cette infection virale respiratoire aiguë provoque une inflammation des parois des bronchioles, c’est-à-dire les plus petites bronches. Généralement, cette pathologie est bénigne, mais “les très jeunes enfants et plus particulièrement les nourrissons de moins de deux mois peuvent présenter une forme plus grave nécessitant une hospitalisation”, selon l’Assurance Maladie. L’EMA a donc déclenché une évaluation accélérée pour ce nouveau vaccin.
Une demande d’autorisation de mise sur le marché pour ce vaccin
Comme le veut la procédure, cette approbation de l’EMA permet au laboratoire de faire une demande d’autorisation de mise sur le marché dans l’Union européenne à la Commission européenne.
“S’il est approuvé, notre candidat vaccin contre le VRS pour les femmes enceintes pourrait aider à protéger les nourrissons immédiatement de la naissance jusqu’à l’âge de six mois, explique le Dr Annaliesa Anderson, directrice Scientifique, recherche et développement des vaccins de Pfizer. Ceci, ainsi que l’approbation pour les personnes âgées, marquerait un progrès significatif en matière de santé publique pour la prévention des maladies à VRS dans toute l’Europe.”
Fin 2022, la Commission européenne avait déjà approuvé un premier traitement capable d’empêcher les formes graves de la maladie chez les nourrissons. Il s’agissait du nirsevimab, vendu sous le nom de "Beyfortus", développé par les laboratoires AstraZeneca et Sanofi.