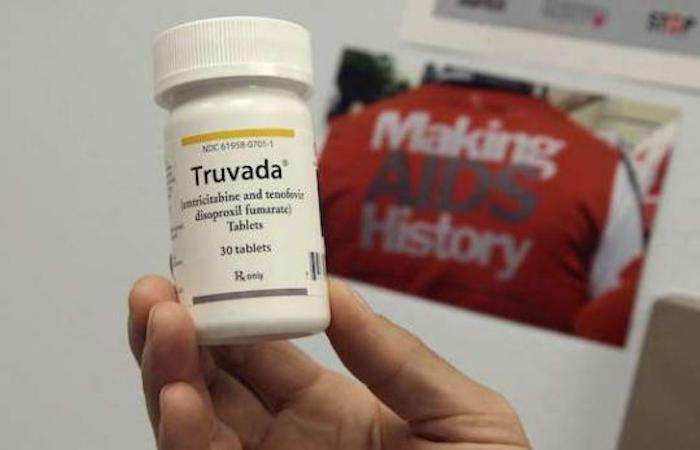
Le traitement préventif du VIH pourrait bien coûter moins cher dans les semaines à venir. Au moins un laboratoire est prêt à distribuer une version générique du Truvada (emtricitabine/ténofovir) : l’Américain Mylan. Comme il l’a annoncé le 26 juillet, une autorisation de mise sur le marché (AMM) européenne lui a été délivrée pour ce médicament indiqué dans le traitement et la prévention d’une infection par le VIH.
Un brevet en fin de course
Trois autres laboratoires sont aussi dans les starting blocks. Biogaran, EG et Zentiva disposent eux aussi de l’autorisation pour produire une version générique du Truvada. Mylan est sans doute le plus avancé : il annonce d’ores et déjà le coût de sa production. La boîte de 30 comprimés reviendra à 179,90 euros. Le princeps, lui, est vendu au prix de 406,86 euros par boîte.
L’économie serait considérable pour l’Assurance maladie. Le Truvada est actuellement pris en charge à 100 % - en prévention comme en traitement de l’infection par le VIH. Et en France, un quart des patients séropositifs reçoivent cette molécule. Des malades auxquels s’ajoutent les quelque 3 000 bénéficiaires de la PrEP déclarés au début de l’année 2017.
Le mois de juillet pourrait bien s’avérer crucial. C’est en effet ce mois-ci qu’expire le brevet du Truvada. Mais comme le précise Gilead, contacté par Pourquoidocteur, « dans les pays où le laboratoire a des Certificats complémentaires de protection (CPP) valides, cela étend nos droits de propriété intellectuelle jusqu’en 2020 ».
La France fait partie des 12 pays sous le coup de cette disposition, qui permet de contourner la limite maximale des brevets, établie à 20 ans. S’enthousiasmer immédiatement serait donc prématuré. D’autant que l’obtention d’une AMM ne préjuge en rien d’une distribution effective, comme l'a précisé l’Agence nationale de sécurité du médicament (ANSM) à Pourquoidocteur.
Un surcoût élevé
Et le laboratoire détenteur du brevet semble bien décidé à se défendre. « Gilead se réserve le droit de protéger et défendre ses droits de propriété intellectuelle en France », a commenté le laboratoire. Une bataille judiciaire est donc à prévoir. Certaines procédures ont d’ailleurs déjà été engagées.
Au Royaume-Uni, plusieurs laboratoires génériqueurs ont attaqué la CPP dont dispose Gilead. Ils soulignent que l’extension du brevet jusqu’en 2020 « conduirait inévitablement à repousser la date de disponibilité des médicaments génériques pour le National Health Service England (Service national de santé, Angleterre) et impliquerait, par là même, des coûts plus élevés ainsi qu’une charge budgétaire plus importante pour ce dernier. »
C’est aussi l’avis des associations. Dans une interview accordée à Libération, Caroline Izambert – exerçant auprès d’AIDES – estime à 815 millions d’euros le surcoût d’une telle prolongation pour les finances françaises.