Responsable d’une grave épidémie en Amérique du Sud et aux Caraïbes en 2016, le virus Zika est connu pour persister de longs mois dans le sperme, et ce bien après que les symptômes aient totalement disparu. Plusieurs études, dont une française, l’avaient démontré.
Mais jusqu’ici, les chercheurs ignoraient comment le virus persistait au sein de l’appareil reproducteur masculin. De nouveaux travaux menés par des chercheurs de l’Inserm et publiés dans la revue Journal of Clinical Investigation apportent des éléments de réponse.
Une persistance du virus dans les cellules germinales
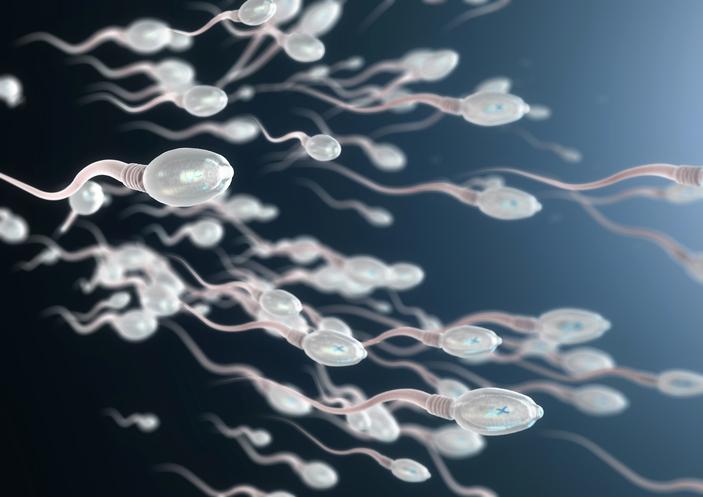
Transmis par les moustiques, le virus Zika est responsable de malformations congénitales chez des enfants à naître, notamment la microcéphalie et le syndrome de Guillain-Barré. Transmissible de l’homme à la femme par voie sexuelle, Zika peut persister dans le sperme pendant plusieurs mois et être transmis plus de 40 jours après la disparition des symptômes, précise l’Inserm dans un communiqué. Lorsque l’appareil reproducteur masculin est infecté, cela a pour conséquences une diminution du nombre de spermatozoïdes et une augmentation des spermatozoïdes anormaux.
L’équipe du Dr Dejucq-Rainsford a montré que pour persister dans le sperme, Zika infecte plusieurs catégories de cellules testiculaires, dont les cellules germinales, à l’origine des spermatozoïdes.
Pour parvenir à cette conclusion, l’équipe de chercheurs a exposé au virus des fragments de testicules d’hommes non infectés, puis les ont maintenus en culture pendant 9 jours afin de suivre l’évolution de l’infection. Les résultats ont ainsi mis en évidence la présence de Zika dans les cellules germinales testiculaires et de spermatozoïdes infectés dans le sperme.
Le testicule, un environnement immunitaire idéal pour Zika
Mais ce n’est pas tout. Les chercheurs ont poussé plus loin les analyses et découvert que le testicule pourrait constituer un "réservoir" pour le virus Zika. En effet, le testicule ne dispose que d’une faible défense immunitaire car il ne produit pas d’interférons, des protéines essentielles à la réponse antivirale et qu’il ne produit qu’en très petites quantités des cytokines pro-inflammatoires, des molécules chargées de signaler la présence de pathogènes au système immunitaire. Par ailleurs, contrairement à d’autres organes, les cellules testiculaires infectées ne meurent pas et perdurent donc dans le testicule, ce qui explique pourquoi on retrouve Zika dans le sperme longtemps après qu’il ait disparu du reste de l’organisme.
Selon les chercheurs de l’Inserm, "l’ensemble de ces éléments pourraient permettre la production de virus au sein du testicule pendant de longues périodes, sans qu’il ne soit éliminé par le système immunitaire".
En observant des modifications du sperme chez des hommes infectés jusqu’à deux mois après contact avec le virus Zika, les scientifiques ont aussi constaté que la production du sperme peut être affectée non seulement par l’infection des cellules germinales, mais aussi par d’autres cellules testiculaires impliquées dans le processus de fabrication des spermatozoïdes (les cellules de Sertolli et les cellules de Leydig), ainsi que celles impliquées dans leur expulsion hors du testicule (les cellules contractiles péritubulaires).
Pour l’équipe du Dr Dejucq-Rainsford, ces travaux fournissent des "informations essentielles sur la manière dont le virus Zika peut persister dans le sperme et en modifier ses paramètres". Ils sont aussi un objet précieux pour tester l’efficacité des agents antiviraux sur l’infection du testicule ex vivo.