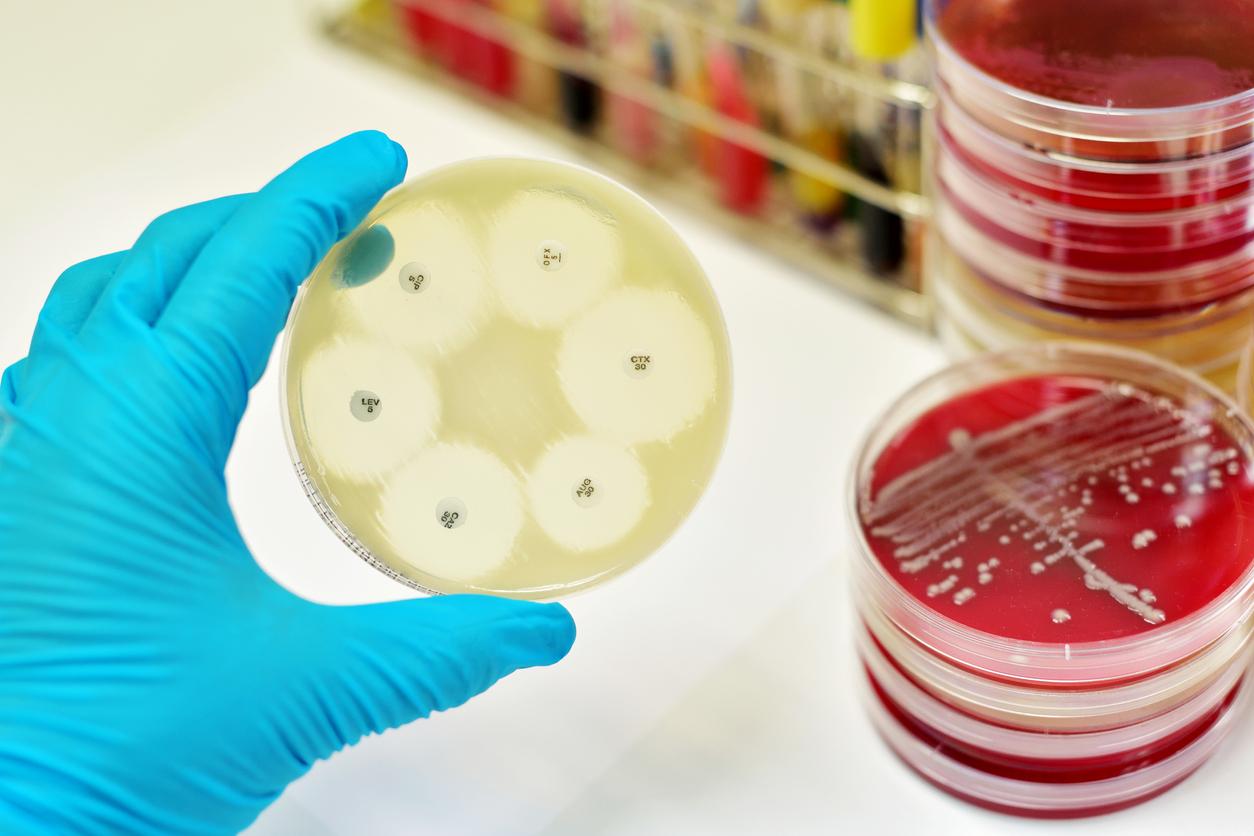
- La découverte des antibiotiques au milieu du XXème siècle a sauvé des millions de personnes d'infections jusque-là incurables
- Mais l'usage intensif de ces médicaments a généré des résistances développées par de nombreuses bactéries
- L'OMS alerte sur la nécessité de développer de nouveaux traitements contre ces bactéries ultra-résistantes
C’est une course dont on ne voit pas encore comment elle pourra s’arrêter et encore moins qui va la gagner. Depuis la découverte du premier d’entre-eux, la pénicilline, les antibiotiques sont régulièrement pris de vitesse par celles qu’ils combattent, les bactéries. Au point que, près de 80 ans après la formidable avancée que leur arrivée a représenté contre les maladies infectieuses, le monde ne croit plus à la capacité de ces médicaments à nous protéger contre les bactéries les plus dangereusement résistantes.
En 1928, le britannique Alexander Fleming qui étudie des staphylocoques voit ses boîtes de culture contaminées par une moisissure qui écarte les bactéries. Ce champignon est appelé « peniucillium notatum » et va révolutionner la médecine : une dizaine d’années plus tard deux autres chercheurs découvrent comment reproduire et stabiliser la pénicilline sous forme médicamenteuse. C’est la naissance des antibiotiques, des substances naturelles ou chimiques qui bloquent la croissance des bactéries ou les détruisent. On estime que ces médicaments ont fait gagner 10 ans de vie à l’humanité en sauvant des millions de personnes d’infections jusque-là incurables comme la tuberculose, la septicémie ou la pneumonie.
6 000 décès par an dus aux bactéries résistantes
Et pourtant, ces médicaments sont aujourd’hui désignés comme responsables d’un nouveau fléau, l’existence de bactéries qui, à force de s’adapter pour survivre aux antibiotiques, sont devenues ultra-résistantes. Au point que les autorités de santé cherchent à limiter l’usage devenu massif des antibiotiques classiques : en 2018, il a été vendu en France 728 tonnes d’antibiotiques pour la santé humaine et 471 tonnes pour la santé animale, ce marché visant pour l’essentiel des espèces consommées par l’homme. Une utilisation tellement large qui aboutit à l’émergence des formes les plus résistantes des bactéries qui causeraient chaque année près de 6 000 décès en France et plus de 30 000 en Europe selon une étude publiée dans The Lancet Infectious Diseases . Si rien ne change, on prédit même que les maladies infectieuses d’origine bactérienne qui avaient été presque vaincues par les antibiotiques redeviendraient en 2050 une des premières causes de mortalité dans le monde en provoquant plus de 10 millions de morts !
Mais la mobilisation contre les effets de l’antibiorésistance est désormais générale. De l’Organisation Mondiale de la Santé aux acteurs du système de santé français, le monde de la médecine sensibilise tous les acteurs pour faire bouger les comportements –en France, ces actions se sont traduites dans la campagne « les antibiotiques, c’est pas automatique »- et développer la recherche pour la mise au point de nouveaux antibiotiques capables de s’attaquer aux « superbactéries ».
Un meilleur usage des antibiotiques
En 2013, l’ANSM (Agence nationale pour la sécurité du médicament) a publié un rapport sur les antibiotiques considérés comme « critiques » et une feuille de route a été définie pour un meilleur usage de ces médicaments : choisir la bonne molécule pendant la bonne durée et uniquement lorsque cela est nécessaire et s’assurer de l’observance des traitements par les patients. Et surtout rappeler des règles d’hygiène simple comme le lavage régulier des mains qui évitent de nombreuses infections et insister sur le fait que les antibiotiques ne doivent pas être utilisés en cas d’infections virales (rhinopharyngites, grippes et bronchiolites, notamment). Ces actions ont abouti à une diminution sur une dizaine d’années de 15% de nombre de prescriptions d’antibiotiques en France.
Faut-il pour autant bannir ces médicaments ? « Sûrement pas, ils sont encore très utiles pour traiter les infections bactériennes, notamment à l’hôpital (7% des prescriptions contre 93% en ville …) ou les infections qui compliquent les maladies virales », prévient le Dr Benjamin Wyplosz, infectiologue au Kremlin-Bicêtre qui reconnait toutefois qu’ils sont « encore trop prescrits en quantité, par exemple dans des infections respiratoires qui guérissent souvent toutes seules comme les bronchites ou les sinusites, ou parfois à mauvais escient avec l’utilisation d’antibiotiques à trop large spectre, notamment dans les infections urinaires ».
40 millions d'euros pour la recherche en France
Pour combattre les résistances, les initiatives se multiplient en matière de recherche. En juillet 2019, une équipe de l’université de Rennes a ainsi testé sur des souris une formule qui ne développait aucune résistance chez les bactéries qu’elle est censée éliminer. Et en juin 2020, des chercheurs du MIT ont mis au point un algorithme capable de repérer les composés antibiotiques dans les médicaments existants qui leur a permis de découvrir qu’un anti-diabètique était capable de paralyser ou de tuer un large spectre d’agents pathogènes redoutés dont celui de la tuberculose.
Et l’innovation est aussi poussée par des actions publiques : la France a lancé en 2018 un programme prioritaire de recherche doté de 40 millions d’euros et dédié à la lutte contre la résistance aux antibiotiques et l’Europe prévoit d’attribuer davantage d’aides sur ce sujet dans le cadre de son programme de recherche « Horizon Europe » planifié jusqu’en 2027.
Une course "infinie" avec les bactéries
Mais la recherche doit aller plus loin : en janvier 2020, l’OMS a diffusé un communiqué pour mettre en garde contre le manque d’innovations permettant de lutter contre les infections résistantes. « Les 60 produits en cours de développement dont 50 antibiotiques apportent peu d’avantages par rapport aux traitements existants et rares sont ceux qui ciblent les bactéries les plus dangereusement résistantes, celles dites à gram négatif », soulignent les responsables de l’OMS en insistant sur le fait que ces bactéries à gram négatif « se propagent rapidement et réclament des solutions de toute urgence ». Si le développement de traitements plus efficaces contre la tuberculose et clostrium difficile responsable de diarrhées sont prometteurs, l'OMS souligne des "lacune inquiétantes" contre la NDM-1, une enzyme résistante à un vaste groupe d'antibiotiques dont ceux appartenant à la famille des carbapénèmes qui sont actuellement le dernier recours contre les infections bactériennes antibiorésistantes.
« Tout n’est pas couvert mais on enregistre des progrès considérables, temporise le Dr Benjamin Wyplosz, les manques sont en partie comblés mais on doit faire face à des bactéries dont le spectre de résistance est incroyable et même avec de nouveaux traitements on observe l’apparition de nouvelles résistances … La course entre les antibiotiques et les bactéries est infinie ! ».
Sujet réalisé à partir du dossier du LEEM "100 questions sur le médicament"
Retrouvez ci-dessous la fiche du LEEM sur le thème "Les antibiotiques, c'est fini?":
https://www.leem.org/100-questions/les-antibiotiques-cest-fini?q=antibiotiques