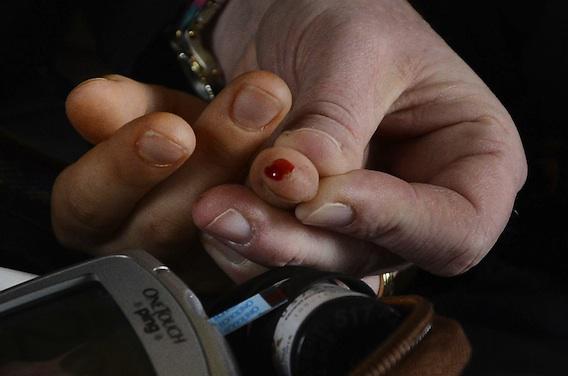
Une start-up de la Silicon Valley a reçu ce jeudi, l’approbation de l’Agence américaine des médicaments (FDA) pour son test détectant le virus de l’herpès à partir d’une simple piqûre au bout du doigt.
La société Theranos, basée à Palo Alto en Californie (Etats-Unis), a orienté toutes ses recherches vers le développement de tests rapides et peu coûteux. Le test ayant reçu l’autorisation de la FDA, nommé HSV-1, coûterait moins de 10 dollars (environ 9 euros), selon l’entreprise.
Celui-ci fonctionne sur le même principe que le test sanguin actuel. Dans un prélèvement sanguin, le test recherche la présence d’anticorps dirigés contre le virus Herpes simplex de type 1 (HSV-1), responsable du fameux « bouton de fièvre », mais aussi de l’herpès génital.
Pour obtenir cette autorisation, Theranos a fourni à la FDA les résultats d’analyses de 818 hommes et femmes.
Un premier pas vers la transparence
« Afin de mettre en œuvre notre vision de la détection précoce, les tests de laboratoire doivent répondre aux critères de qualité les plus élevés – des standards fixés par la FDA, a expliqué dans un communiqué Elizabeth Holmes, fondatrice et directrice générale de Theranos.
L’examen de l’Agence est l’unique processus rigoureux auquel nous voulions nous plier car nous sommes déterminés à veiller à ce que nos systèmes et tests soient de grande qualité, et que les patients et les médecins aient accès aux informations les plus précises concernant leur santé. Nous nous réjouissons à l’idée de poursuivre notre relation solide avec l’Agence. »
Une annonce qui sonne comme un règlement de comptes. Selon le Washington Post, la société est régulièrement accusée de manquer de transparence. Ils évoquent notamment un éditorial signé par John Ioannidis, président du département de prévention à l’université de Stanford, dans la revue JAMA en février. L’autorisation de la FDA devrait lever le voile sur certaines pratiques de l’entreprise, selon ce dernier.