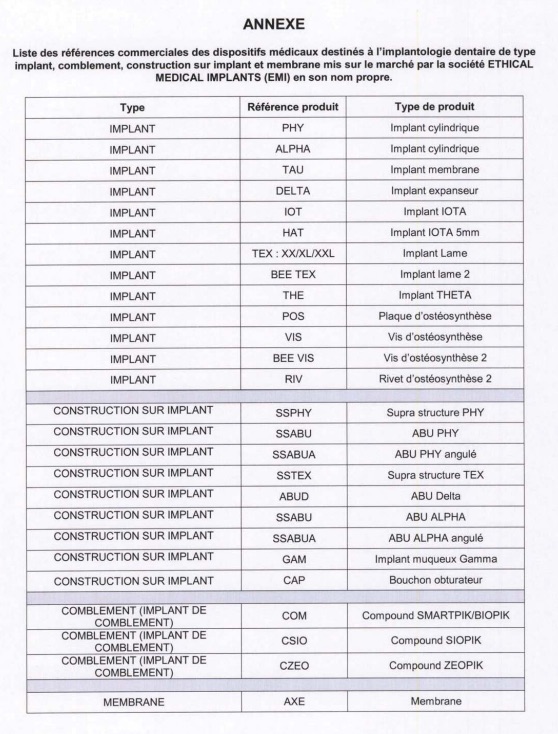
Des implants pour le moins suspects. L’ANSM (Agence nationale de sécurité du médicament) a suspendu la mise sur le marché et la fabrication de dispositifs médicaux conçus par la société Ethical Medical Implants (EMI), basée à Mérignac (Gironde). Les matériaux concernés sont des implants, comblements, constructions sur implant et membranes, tous destinés à l’implantologie dentaire.
Dans sa décision de police sanitaire (DSP), l’agence indique avoir mené une inspection en novembre 2016 dans les locaux près de Bordeaux. Les inspecteurs ont alors découvert que la matière première à partir de laquelle les implants étaient fabriqués n’aurait jamais dû être utilisée à des fins médicales.
"Not for human implantation"
« L’emballage de la matière première de référence VESTAKEEP 4000P retrouvée en stock sur le site de la société EMI portait un étiquetage jaune avec une mention traduisant l’interdiction d’utiliser en l’état cette matière première en implantologie humaine (« this material is not for human implantation ») », note l’ANSM.
Les implants sont conçus à partir de polyétheréthercétone (PEEK), une matière utilisée à des fins médicales après avoir été reconditionnée pour cet usage. Sauf qu’en l’état, la référence VESTAKEEP 4000P « figure sur la liste des matières premières destinées à une utilisation industrielle », et non médicale – et encore moins en implantologie.
Biocompatibilité et toxicité
En l’état, rien ne permet de garantir la biocompatibilité de ce dispositif médical qui n’en est pas un, ni sa toxicité. Et ce, alors que de tels dispositifs doivent être fabriqués selon des procédures strictes « pour la compatibilité réciproque entre les matériaux utilisés et les tissus, cellules et liquides corporels », et afin de « minimiser le risque que présentent les contaminants et les résidus ». Les données cliniques et précliniques fournies par la société n’ont pas permis de « démontrer les performances de sécurité et de santé » du matériel.
Par ailleurs, l’ANSM note des défaillances dans le processus de stérilisation et de stockage des dispositifs. L’agence demande au fabricant de procéder au retrait du marché des produits visés et de contacter les professionnels et les entreprises susceptibles de détenir ces produits.
Selon le site societe.com, l’entreprise Ethical Medical Implants est une très petite structure, de trois à cinq salariés, dont le chiffre d’affaires en 2015 s’est établi à 7 000 euros. Pas de quoi irriguer le marché français, donc. Contactée, l'agence indique que concernant le risque, celui-ci a été évalué pour les patients déjà implantés. Des éléments transmis à l'ANSM ont permis de démontrer l'absence de risque de toxicité de la matière première utilisée. Par ailleurs, l'ANSM n'a pas de signalement de matériovigilance concernant ce dispositif médical.