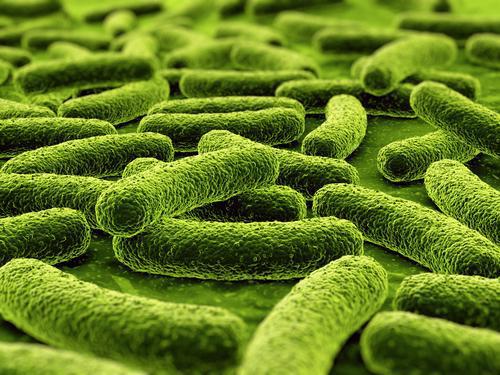
« C’est dans la tête ». Voilà ce qu’on rétorque fréquemment aux personnes qui se plaignent de fatigue chronique. Une réponse insuffisante qui n’aura bientôt plus raison d’être. Des chercheurs de l’université de Cornell ont trouvé une nouvelle méthode de diagnostic plus rapide et non-invasive. Les patients rapportent fréquemment des symptômes gastro-intestinaux : l’idée a donc germé chez les chercheurs d’étudier leur flore intestinale. Ils ont analysé des échantillons de sang et de selles.
Jusque-là, les tests longs et nombreux laissaient les patients dans l’errance diagnostique pendant des années. La maladie est en effet mal connue : elle se caractérise par une fatigue intense déclenchée par un effort dit « normal » et qui n’est pas soulagée par le repos. Et elle est encore souvent associée à des causes psychiques.
Moins de bonnes bactéries
Les chercheurs américains ont séquencé l’ADN de la flore intestinale de 48 patients atteints de fatigue chronique et de 39 sujets sains. Ils ont montré que les souches bactériennes étaient moins diversifiées chez les premiers que chez les seconds. Les scientifiques ont aussi dénombré chez les patients moins de bactéries anti-inflammatoires et plus de bactéries pro-inflammatoires, comme c’est le cas dans d’autres affections telles que la maladie de Crohn.
Les analyses sanguines des personnes atteintes de fatigue chronique montrent également des taux de marqueurs de l'inflammation anormalement hauts. Les scientifiques émettent l’hypothèse que les bactéries présentes dans l’intestin franchiraient sa paroi. Elles se retrouveraient alors dans la circulation et aggraveraient les symptômes des malades.
Impossible pour l’instant cependant de déterminer si la faible diversité bactérienne est une cause ou une conséquence de la maladie. Mais Ludovic Giloteaux, premier auteur de l’étude, estime que, grâce à ces données, « les cliniciens pourraient envisager un régime alimentaire avec des probiotiques (des bactéries bénéfiques pour les intestins), des fibres alimentaires, et des prébiotiques (aliments qui favorisent la croissance ou l’activité des « bonnes » bactéries) ». Prochaine étape : chercher des preuves de virus et champignons qui pourraient s’associer aux bactéries et contribuer aux symptômes.